► Inhaltsverzeichnis Kapitel (ausklappbar)
- Gründe für Ausbruchsuntersuchung
- Bausteine der Ausbruchsuntersuchung
- Baustein: Ausbruch bestätigen
- Baustein: Teambildung und -strukturierung
- Baustein: Diagnose sichern
- Baustein: Falldefinition erstellen
- Baustein: Weitere Fälle suchen
- Baustein: Ausbruch beschreiben
- Baustein: Hypothese entwickeln
- Baustein: Hypothese prüfen
- Baustein: Maßnahmen ergreifen
- Baustein: Kommunizieren
Die beiden Begriffe Ausbuchsmanagement und Ausbruchsuntersuchung wurden, und werden, zum Teil synonym und zum Teil unterschiedlich verwendet. Im Folgenden verstehen wir unter Ausbruchsmanagment “alle Aufgaben, die eine weitere Verbreitung einer Infektionskrankheit wirkungsvoll und zügig zu verhindern”. (KRINKO, 2002)
Unter Ausbruchsuntersuchung verstehen wir “die zielgerichtete infektions-epidemiologische Untersuchung die die Bedrohung für die Bevölkerung ermittelt, die Infektionsquelle identifiziert und Maßnahmen ergreift, um Folgefälle und ähnliche Ausbrüche in der Zukunft zu verhindern. (“Ausbruchsuntersuchungen,” 2014)
Gründe für Ausbruchsuntersuchung
Die Lachsschaumspeise
Im Monty Python Film “Der Sinn des Lebens” gibt es eine Szene, in der Freunde beim gemeinsamen Abendessen von “Mr. Death”, dem Tod, besucht werden. Er teilt ihnen mit, dass sie alle gestorben sind und er sie jetzt mitnimmt. Einer der Gäste frägt “Warum sind wir gestorben?”, woraufhin seine Knochenhand auf eines der Gerichte zeigt: “Die Lachsschaumspeise!”. Einer der Gäste wundert sich noch “Ich hab’ die doch gar nicht gegessen?!?”, bevor alle auf dem Tisch zusammenbrechen um dann als Geister in ihre Geisterautos steigen und Mr. Death ins Jenseits folgen.
“Woran sind Menschen im Ausbruch erkrankt und wie kann ich den Ausbruch stoppen?” sind die Leitfragen für die Durchführung von Ausbruchsuntersuchungen. Direkt daraus leitet sich dann oft die praktische Intervention ab: beispielsweise Lebensmittelrückruf, die Durchführung von Impfungen und Chemoprophylaxe und Barrieremaßnahmen, Identifizierung von Schulungsbedarf oder Erkennen von Hygienebrüchen (#?HACCP) (#hier Verweis auf Kapitel Intervention#). Man möchte die Quelle des Ausbruchs finden und für die Zukunft beseitigen, damit nicht noch mehr Menschen krank werden.
Manchmal findet man auch einen bisher unbekannten Erreger, wie z.B. Legionellen, HIV, Ebola oder zuletzt SARS und SARS-CoV II. Ohne strukturierte Ausbruchsuntersuchungen, die über die Einzelpatienten hinaus die erkrankte und nicht-erkrankte Population miteinander vergleichen, wären diese Erreger nie so schnell entdeckt worden.
Eine weitere Motivation für eine Ausbruchsuntersuchung ist der äußere Druck durch die Medien oder positiver formuliert: das Eingehen auf die Sorgen und Ängste der lokalen Bevölkerung. Die Entscheidung, welcher der über 100 Norovirenausbrüche pro Saison im Kreis jetzt untersucht wird, wird oft durch die Berichterstattung der Zeitungen oder Onlinemedien bestimmt. Ein Ausbruch, über den in einer regionalen Zeitung mehrfach berichtet wird, kann so viel Druck bei den politisch Verantwortlichen im Kreis und Landesministerium erzeugen, dass die zuständigen Gesundheitsbehörden nicht um eine strukturierte Untersuchung herumkommen.
Der einzige Top-Experte im Amt nutzt nichts, wenn er im Urlaub ist. Die Veteranin im Gesundheitsamt hat hoffentlich vor der Altersteilzeit ihr Wissen der nachfolgenden Generation weitergeben. Nein? Wieder von vorne anfangen? Eine letzte sehr wichtige Motivation für die Durchführung von Ausbruchsuntersuchungen ist das Lehren und Lernen von praktischer Ausbruchsepidemiologie.
Bausteine der Ausbruchsuntersuchung
Das Vorgehen bei Ausbruchsunterschungen kann in mehr oder weniger destinkte Aktivitäten unterteilt werden. Diese Aktivitäten werden häufig in ungefähr 10 “Arbeitsschritten” aufgeführt, die meistens parallel und nicht in zeitlicher Abfolge ablaufen. Da es dabei nicht immer einen strengen chornologischen Ablauf gibt, finden wir es angebrachter, diese Aktivitäten nicht als Schritte, sondern als Bausteine im Sinne eines Puzzles, einer Ausbruchsuntersuchung zu betrachten, die meistens gleichzeitig ablaufen können:

(Bensyl, Goodman, & Rasmussen, n.d., pp. 6–2)
Baustein: Ausbruch bestätigen
Zur Identifizierung von Clustern (und Ausbrüchen) dient der Vergleich mit einer Hintergrundrate. Dieser ist relativ einfach herzustellen, wenn Surveillance-Daten zur Häufigkeit von bestimmten Infektionen bereits vorhanden sind. Solche Daten können auch aus Literaturangaben stammen, z. B. die zu erwartende Häufigkeit von MRSA-Nachweisen in den letzen Jahren in einer neonatologischen Klinik. Allerdings muss verifiziert werden, welche Definitionen den Routinedaten zugrunde liegen und ob mit ausreichender Sensitivität und Spezifität erfasst wurde.
Bereits zu diesem Zeitpunkt sollten verfügbare Informationen gesammelt werden:
-
Zeitpunkt und Ort des Auftretens des auffälligen Ereignisses
-
Informationen zu den betroffenen Personen (Linelist anlegen)
-
Informationen zum Erreger oder zum Krankheitsbild
-
Vorliegen von Risikofaktoren (Immunsuppression, hohes Alter, Begleiterkrankungen, spezielle berufliche Exposition)
-
die äußeren Umstände (Hitzewelle, im Krankenhaus z.B. Überbelegung und Personalmangel )
Wenn die Frage: “Gibt es mehr Fälle als räumlich und zeitlich zu erwarten wären und stehen diese in einem epidemiologischen Zusammenhang?” mit ja beantwortet werden kann, dann liegt ein Ausbruch vor. Bei komplexen und protrahierten Ausbrüchen muss diese Frage im Verlauf mehrmals gestellt werden. Der Ausbruchsverdacht sollte zu Ermittlungen führen, in deren Rahmen sich herausstellen kann, dass kein Ausbruch vorliegt. Ein einzelner Fall kann bereits Grund für einen Ausbruchsverdacht sein und eine Ausbruchsuntersuchung nach sich ziehen (z.B. ein einzelner Nachweis von Ebola, Lassa oder Botulismus in Deutschland).
Neue Verfahren, wie die molekulare Surveillance und digitale Epidemiologie unterstützen vor allem bei der Identifizierung überregionaler Ausbruchsgeschehen (beispielsweise Listeriose-Ausbrüche) und bei nosokomialen Ausbrüchen (“Allgemeine Verwaltungsvorschrift über die Koordinierung des Infektionsschutzes in epidemisch bedeutsamen Fällen (IfSGKoordinierungs-VwV),” 2013).
Ermittlungen in einem Ausbruch
Der gesamte Ausbruchsverlauf einschließlich eingeführter Infektionsschutz-Maßnahmen sollte beispielsweise in einem Protokoll dokumentiert werden. Die Befundinterpretation erfolgt überwiegend durch die Mitarbeiter des Gesundheitsamtes. Dabei sollte ein Ermittlungsbogen gemäß § 25 IfSG mit folgenden Daten ausgefüllt werden:
-
Vor- und Nachname,
-
Geburtsdatum,
-
Adresse,
-
Telefonnummer der betroffenen Person,
-
seine berufliche Tätigkeit (z. B.: Lebenmittelberuf, Mitarbeiter einer Gemeinschaftseinrichtung),
-
dem Erkrankungsbeginn,
-
die erste Arztkonsultation,
-
die Symptomatik,
-
den Krankenhausaufenthalt (von/ bis) und
-
die Infektionsquelle - sollte diese bekannt sein.
Kontaktpersonen
während eines Ausbruchs kann es notwendig sein, Kontaktpersonen zu ermitteln. Hierbei sind folgende personenbezogene Daten durch den Mitarbeiter des Gesundheitsamtes zu ermitteln:
-
der Vor- und Nachname,
-
das Geburtsdatum,
-
die Adresse und
-
die Telefonnummer, E-Mail.
Baustein: Teambildung und -strukturierung
Die Zusammensetzung des Ausbruchsteams richtet sich nach den besonderen Erfordernissen des jeweiligen Ausbruchs und weist damit eine gewisse Variabilität auf. Eine Übersicht über zentrale Rollen, welche bei jedem Ausbruch anfallen ist in tabellarischer Form im Folgenden dargestellt. Darüber hinaus können je nach Art der Ausbruchs weitere Aufgaben hinzukommen, welche in nachfolgenden Kapiteln weiter charakerisiert werden. Zur Aufgabe der leitenden Person eines Ausbruchsteams gehört es sicherzustellen, dass alle benötigte Aufgaben erfüllt werden können. Um dies zu gewährleisten bietet es sich an eine Übersicht über die zu leistende Arbeit heranzuziehen, z.B. im Kapitel 2 eingeführte Aktivitätenliste der PSP (Projektstrukturplan). Jeder Aktivität der Aktivitätenliste wird im Folgenden eine konkret verantwortliche Person zugeordnet. Diese Person trägt die Verantwortung für die Erfüllung des Arbeitspakets und ist verantwortlich für regelmäßige Statusberichte an die Leitung. Auf diesem Weg wird eine Verantwortungsdiffusion verringert und eine doppelte Bearbeitung einzelner Arbeitsschritte verhindert.
Bei einem Ausbruch ist es wichtig, die für die Durchführung von Kontrollmaßnahmen verantwortlichen Personen, frühzeitig in das Team einzubinden und von ihrer Verantwortung zu überzeugen. Bei nosokomialen Ausbrüchen ist beispielsweise häufig der Ärztliche Direktor verantwortlich für die Hygiene im Krankenhaus und sollte daher frühzeitig eingebunden werden. Das Ausbruchsteam besteht folglich nicht immer lediglich aus Mitglieder der bearbeitenden Behörden, sondern kann auch externe Akteure mit einbeziehen.
Dokumentation von Treffen
Um Absprachen und wichtige Entscheidungen zu dokumentieren ist es wichtig dass von relevanten Treffen Dokumentationen angefertig werden.
Vorlage: Protokoll Teamtreffen
Titel (z.B. ”Treffen Team Ausbruchsuntersuchung”)
Datum, Zeit und Ort
1. Festlegen: Vorsitz, Protokoll, Zweck des Treffens
2. Anwesende, entschuldigte Teilnehmende
3. Agenda (erstellen)
4. Protokoll der vorangegangenen Sitzung
5. Standortbestimmung / Überprüfung der Evidenz
- Epidemiologisch
- Mikrobiologisch
- Umwelt- und Nahrungsmittelkette
6. Aktuelle Risikobewertung
7. durchgeführte Kontrollmaßnahmen
8. Weitere geplante Untersuchungen
- Epidemiologisch
- Mikrobiologisch
- Umwelt- und Nahrungsmittelkette
9. Kommunikation / Mitteilungen an
- Öffentlich
- Medien
- Leistungserbringer im Gesundheitswesen (z.B. Hausärzte, Krankenhäuser etc…)
- Andere
10. Aufgaben, Verantwortliche und Zeiträume bestimmen
11. Verschiedenes
12. Datum der nächsten Sitzung
Baustein: Diagnose sichern
Zu Beginn einer Ausbruchsuntersuchung, aber auch im Verlauf, sollte überprüft werden, ob oder in welchem Ausmaß das Geschehen auf klinisch oder labordiagnostische Unsicherheiten zurückzuführen sein könnte. Verändertes Testverhalten, oder Testverfahren, Veränderungen in der Aufmerksamkeit von Ärzten/Ärztinnen können zu Nachweishäufungen führen, sogenannten Pseudoausbrüchen.
KASTEN Beispiel: Blutspender werden zunehmend auch auf Hepatitis-E gescreent. Durch die Labormeldepflicht erhöht sich dadurch die Fallzahlen im Vergleich zu den Vorjahren, ohne dass ein Ausbruch vorliegt.
Bei Pseudoausbrüchen handelt es sich nicht um tatsächliche Erkrankungs- oder Erregerhäufungen, sondern um Häufungen von deren Nachweis. Ziel dieses Bausteins ist es, so früh wie möglich differenzieren zu können zwischen Ausbruch und Pseudoausbruch. Dazu eigenen sich folgende Maßnahmen:
-
Klinische Diagnostik: durch systematische Patientenuntersuchungen und Hinzuziehung von Experten können Unsicherheiten reduziert werden. Häufig ist eine systematische Auswertung einzelner Patientenakten oder von Arztbriefen ausreichend.
-
Patienteninterviews oder Interviews von Behandlungspersonals sind ebenfalls sehr hilfreich, um nachzuvollziehen, ob ähnliche Erkrankungssymptome vorliegen oder nicht.
-
Klinische Proben und Materialien, die möglicherweise mit dem Ausbruch in Verbindung stehen, müssen schnellstmöglich untersucht werden und sollten aufbewahrt werden, bis geklärt ist, ob weiterführende Untersuchungen notwendig sind.
-
Bei bereits durchgeführten Untersuchungen sollten die verwendeten Methoden abgeklärt werden: welches Probenmaterial, welche Entnahmetechnik, Transport (Temperatur? Kontaminationsmöglichkeit? etc.), Versand, Labormethoden. Nationale Referenzzentren und Konsiliarlabore können bei der Evaluation der Erregerdiagnostik im Ausbruchsfall unterstützen (https://www.rki.de/DE/Content/Infekt/NRZ/nrz_node.html).
-
Erregertypisierung: Im Rahmen einer Ausbruchsuntersuchung können Typisierungsverfahren von Erregern unterhalb der Speziesebene eine sinnvolle und notwendige Ergänzung sein, wenn sie dazu dienen, die Sicherung der Diagnose oder/und Falldefinition zu ermöglichen oder Transmissionsketten aufzuklären. Bei der Aufklärung lebensmittelassoziierter Infektionen kann die Erregertypisierung zum Abgleich von Human- und Lebensmittelisolaten eingesetzt werden. Eine Typisierung muss nicht in jedem Fall durchgeführt werden; z.B. kann bei seltenen Erregern oder ohnehin eindeutigen Falldefinitionen auf eine Typisierung verzichtet werden.
Zu beachten: Es gibt kein 100% ideales Typisierungsverfahren und es gibt Ausbrüche bei denen in der Infektionssquelle oder auf dem Vektor mehrere Erregerstämme oder Erregerspezies vorkommen (Multispeziesausbrüche).
Baustein: Falldefinition erstellen
Für jede Ausbruchsuntersuchung wird eine Falldefinition erstellt. Die Falldefinition ist ein Instrument, anhand dessen standardisiert und nachvollziehbar entschieden werden kann, welche Erkrankungsfälle dem Ausbruch zugeordnet werden und welche nicht.
Wichtig: Die Ausbruchsfalldefinition ist nicht dasselbe wie die Falldefinition, die vom RKI für die Übermittlung von Erkrankungsfällen erstellt werden.
Zu Beginn der Ausbruchsuntersuchung ist die Falldefinition sensitiv, das heißt, es sollen möglichst viele Erkrankungsfälle, die zum Ausbruch gehören, erfasst werden [Bsp. Falldefintion siehe unten: Kinder mit gastrointestinalen Symptomen]. Dafür nimmt man in Kauf, dass vielleicht auch Erkrankungsfälle erfasst werden, bei denen sich später, z. B. mit entsprechender Labordiagnostik, herausstellt, dass sie doch nicht zum Ausbruch gehören (Falsch-Positive) [im Bsp. Falldefintion siehe unten: Kinder, die aus anderen Gründen Bauchschmerzen hatten]. Die Ausbruchsfalldefinition ist flexibel und kann sich im Verlauf der Ausbruchsuntersuchung ändern, wenn neue Erkenntnisse gewonnen werden, die eine Anpassung der Falldefinition erforderlich machen.
Im Verlauf der Ausbruchsuntersuchung kann sie zunehmend spezifischer werden. Mit einer spezifischen Falldefinition werden nur die Erkrankungsfälle erfasst, die wirklich zum Ausbruch gehören und die, die nicht zum Ausbruch gehören, können ausgeschlossen werden. Eine Falldefinition basiert auf objektiven Kriterien (z.B. klinische Symptome, labordiagnostische Ergebnisse), und sollte immer die epidemiologischen Aspekte Zeit, Ort, Person (ZOP) enthalten. Unter dem Aspekt Zeit wird beschrieben, wann die Erkrankungsfälle, die dem Ausbruch zugerechnet werden sollen, aufgetreten sind. Unter dem Aspekt Ort wird beschrieben, wo die Erkrankungsfälle aufgetreten sind (z.B. Landkreis XY, Schule Z in Landkreis XY, Firma A). Unter dem Aspekt Person werden die betroffenen Personen (z.B. Schülerinnen und Schüler der Klasse 4c) und häufig auch deren Symptome beschrieben (z.B. Schülerinnen und Schüler der Klasse 4c mit Durchfall und/oder Bauchschmerzen).
Beispiel Falldefinition: Als Fälle des Ausbruchs werden Schülerinnen und Schüler der Klasse 4c bezeichnet [PERSON] der XY-Schule in Z [ORT], die in den 7 Tagen nach dem Besuch der Schulklasse 4c auf dem Bauernhof X an x.x.20xx [ZEIT]mit Durchfall und/oder Bauchschmerzen erkrankt [PERSON] sind.
Beispiel für eine spezifischere Falldefinition: Als Fälle des Ausbruchs werden Schülerinnen und Schüler der Klasse 4c bezeichnet [PERSON] der XY-Schule in Z [ORT], die in den 7 Tagen nach dem Besuch der Schulklasse 4c auf dem Bauernhof X an x.x.20xx [ZEIT]mit Durchfall und/oder Bauchschmerzen erkrankt sind und bei denen labordiagnostisch eine Campylobacter-jejuni-Infektion nachgewiesen wurde [PERSON] .
In Ausbruchsuntersuchungen unterscheidet man häufig die Fallkategorien Verdachtsfälle/mögliche Fälle, wahrscheinliche Fälle und gesicherte/bestätigte Fälle. Für jede Fallkategorie muss eine Falldefinition erstellt werden.
Baustein: Weitere Fälle suchen
Auf der Grundlage der bisher gewonnen Daten und mit Hilfe der Falldefinition müssen weitere Fälle ermittelt werden. Dies ist insbesondere dann wichtig, wenn es sich um schwerwiegende Erkrankungen handelt und wenn der Erkrankungserreger von Person zu Person übertragen werden kann. Insbesondere bei Personen zu Personen Übertragungen in Krankenhäusern, können die Infektionsschutzmaßnahmen nur dann erfolgreich sein, wenn alle Fälle identifiziert wurden. Bei anderen Ausbrüchen, kann es ausreichend sein, im Verlauf der Untersuchung Erkenntnisse zu sammeln, wie groß die aktuelle Unterschätzung der Fallzahlen sein könnte (eher Faktor 2 oder 10?) (Haagsma et al., 2013).
Je nach Krankheitsbild oder Erreger benötigt man eine Strategie zur Fallsuche: Wenn es relevant ist, auch symptomlose Personen, also alle Träger und Trägerinnen bzw. alle Kolonisierten zu identifizieren, dann müssen systematische Untersuchungen durchgeführt werden. Dazu muss die zu untersuchende Gruppe sinnvoll gewählt und Screeninguntersuchungen organisiert werden. Dies sollte in enger Abstimmung mit den beteiligten Laboren erfolgen. Als Screeninguntersuchungen kommen z.B. auch seroepidemiologische Untersuchungen in Frage.
Alle Daten sollten mit Hilfe eines standardisierten Erfassungsbogens erfasst werden. Damit soll sichergestellt werden, dass keine wichtigen Informationen vergessen werden und beispielsweise Kranken-, Labor- und sonstige Akten nicht mehrmals durchgesehen werden müssen. Die zu sammelnden Informationen umfassen demographische Daten (Identifikation des Falles, Geburtsdatum, Geschlecht), klinische Symptomatik (Art, Beginn, Ende, Ausprägung, betroffene Körperbereiche), gegebenenfalls das Datum der Krankenhausaufnahme, evtl. auch der Krankenhausentlassung, der Station (bei mehreren Stationen: Daten des Aufenthaltes auf jeder Station), relevante Laborbefunde (Datum der Entnahme, Art der Proben, untersuchendes Labor, evtl. angewandte Methode, Ergebnis) und Grundkrankheiten des Patienten. Grundkrankheiten des Patienten.
Baustein: Ausbruch beschreiben
Zu Beginn einer Ausbruchsuntersuchung werden Erkrankungsfälle wenn möglich ausführlich befragt, um Gemeinsamkeiten zwischen den Erkrankungsfällen zu finden und dadurch die Ausbruchsursache zu ermitteln (explorative bzw. Hypothesen-generierende Befragungen, alternativ: ”Shotgun-Fragebogen” (sehr ausführlicher Fragebogen, der zur Hypothesen-Generierung bei Lebensmittelbedingten Ausbrüchen genutzt werden kann). Eine deutsche Version des Shotgun-Fragebogens kann beim RKI angefordert werden (“Shotgun-Questionnaire,” 2014). Bei nosokomialen Ausbrüchen werden normalerweise Informationen aus Arztbriefen Krankenakten oder der Krankenhausinformationssystem systematisch erhoben und für die Hypothesengenerierung genutzt. Erhobene Informationen über die Erkrankungsfälle werden systematisch dokumentiert (Linelist #Verweis auf Grundlagen einfügen).
Alle vorliegenden Informationen zum Ausbruch werden zur Ausbruchsbeschreibung geordnet, wobei wieder die Aspekte Zeit, Ort und Person (ZOP) berücksichtigt werden.
Unter dem Aspekt Zeit wird beschrieben, wann der Ausbruch stattgefunden hat. Dafür wird eine Epidemiekurve erstellt, die grafisch die Anzahl der Erkrankungsfälle nach der Zeit ihres Auftretens darstellt. Auf der X-Achse der Epidemiekurve kann z.B. der Erkrankungsbeginn (Tag) dargestellt sein, auf der Y-Achse die Anzahl der Fälle, die an dem jeweiligen Tag erkrankt sind.
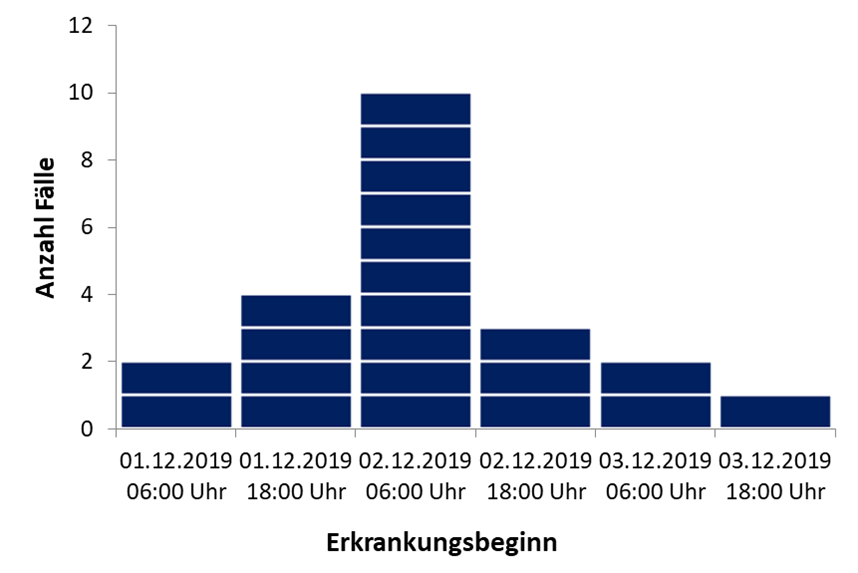
Die Epidemiekurve ist für die Ausbruchsuntersuchung ein wichtiges Instrument. Anhand der Epidemiekurve kann die Dynamik und das Ausmaß des Ausbruchs dargestellt werden (Punktquelle oder fortbestehende Infektionsquelle). Statistisch betrachtet ist eine epidemische Kurve ein Histogramm der aufgetretenen Fälle entlang der Zeitachse. Die Wahl der Zeiteinheiten (engl. “histogram bucket size”) ist nicht festgelegt und hängt von Erreger und Darstellungsziel ab. Für die Beschreibung der jährlichen Erregerdynamik von z.B. Salmonellen oder Campylobacter genügt ein wöchentlicher Zeitabstand. Im Ausbruch gelingt die Abbildung der Dynamik gut, wenn man die halbe Inkubationszeit (Median, #Verweis Anhang Tabelle Inkubationszeiten) als Zeitabstand nimmt, um keine Sprünge in den Erkrankungen zu verpassen. Für eine Darstellung der Krankheitsübersicht am Ende des Ausbruchs würde man größere Zeitabstände verwenden, um auf gleicher Darstellungsfläche mehr Fälle abbilden zu können.
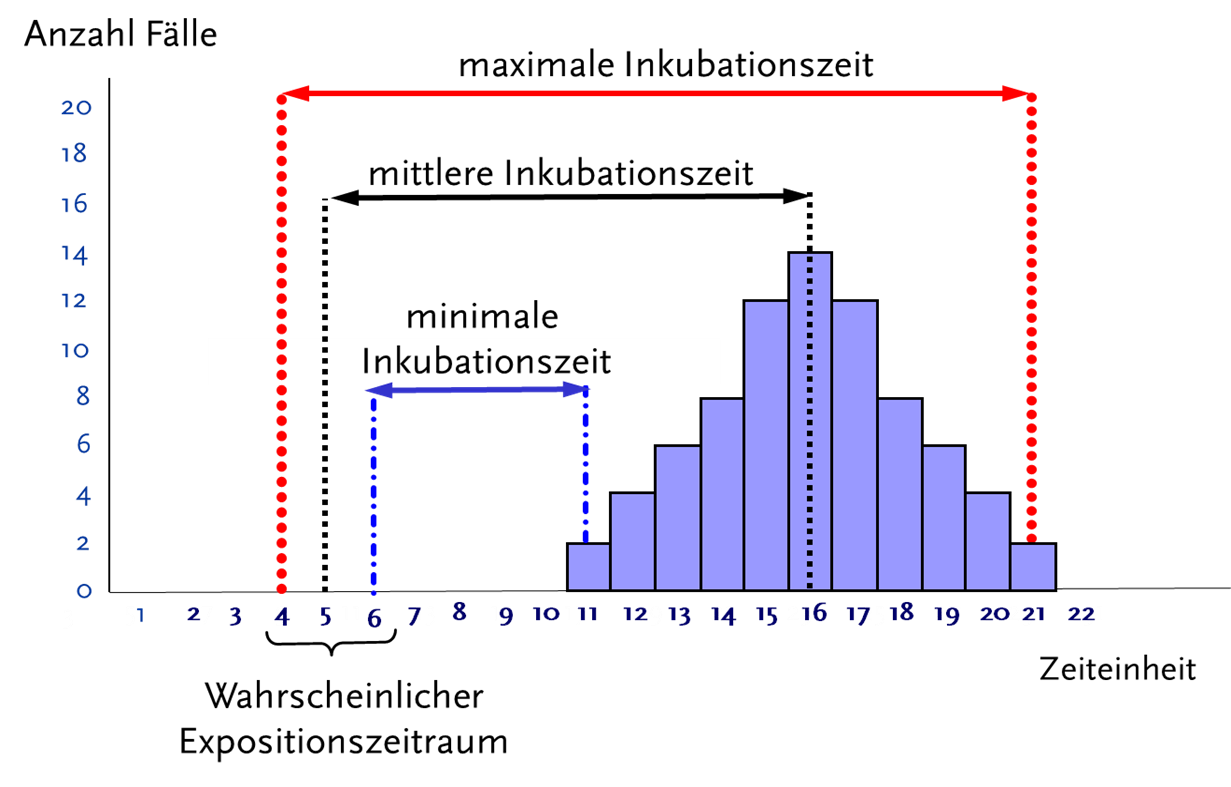
Auch kann die Form der Epidemiekurve wertvolle Hinweise auf den Übertragungsweg des Erregers liefern (z.B. Mensch-zu-Mensch-Übertragung). Anhand der Epidemiekurve kann u.U. der mögliche Infektionszeitraum bestimmt werden, wenn der Erreger und die Inkubationszeiten bekannt sind (bitte hier internen Link einfügen AUS05 “Inkubationszeite ausgewählter gastroenterischer Erreger). Wenn der genaue Expostionszeitpunkt der Erkrankungsfälle bekannt ist (z.B. eine Familienfeier) aber der Krankheitserreger noch unbekannt ist, kann anhand der Epidemiekurve die Inkubationszeit für den Erreger abgeschätzt und damit zusätzliche Hinweise auf den Erreger erlangt werden.
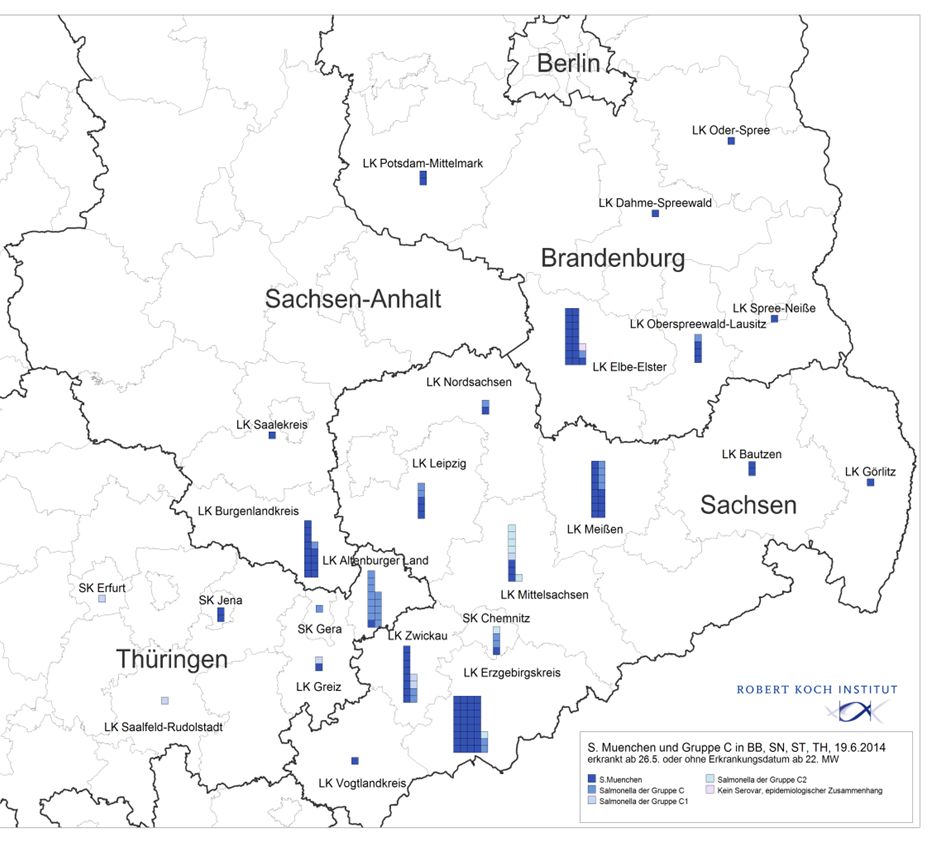
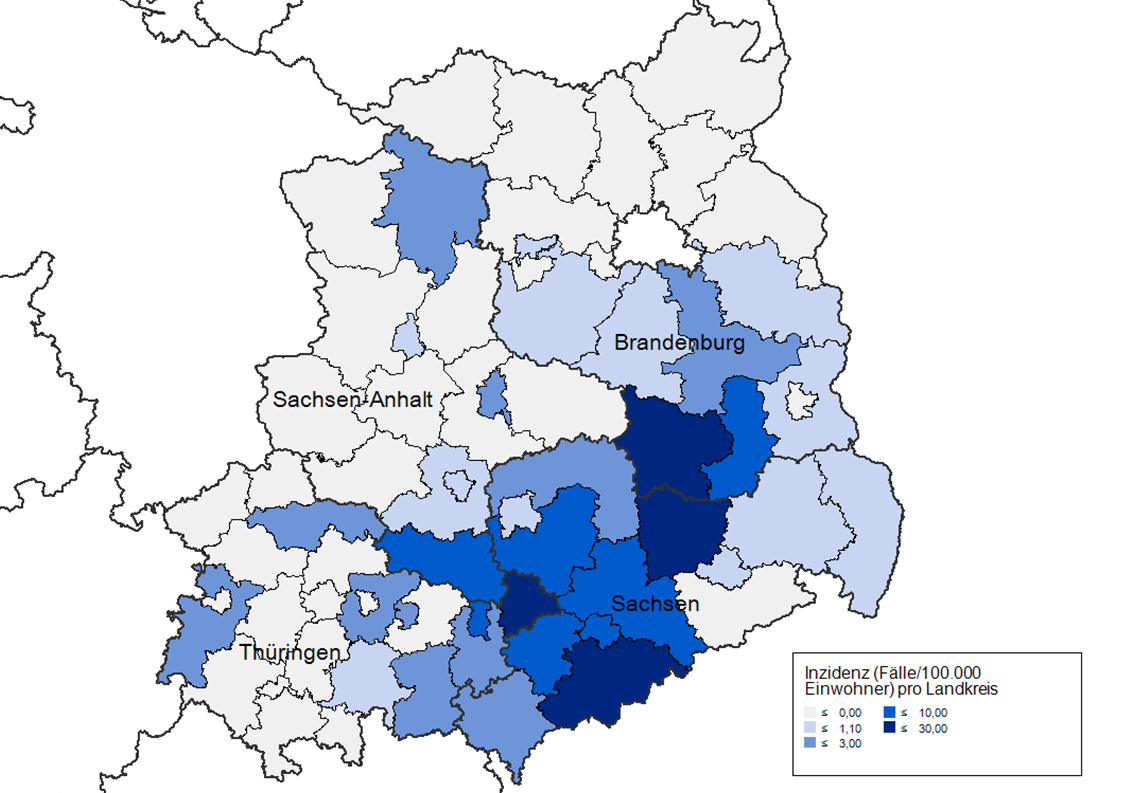
Unter dem Aspekt Ort wird beschrieben, wo sich der Ausbruch ereignete. Eine Darstellung mit Landkarten, auf der die Orte, wo Fälle aufgetreten sind, dargestellt werden, kann hilfreich sein (Punktkarte; pro Erkankungsfall ein Punkt). Dabei ist zu beachten, dass aus Datenschutzgründen nicht die genauen Wohnorte der Erkrankungsfälle zu erkennen sein sollte. Eine Inzidenzkarte, auf der die Inzidenzen, z.B. in verschiedenen Landkreisen, farblich kodiert dargestellt werden, ist eine andere Darstellungsmöglichkeit.
Unter dem Aspekt Person werden die vorliegenden Informationen über die Erkrankungsfälle beschrieben. Dazu gehören Geschlecht und Alter (Altersdurchschnitt, Altersspanne, ggf. Altersgruppen) der Erkrankten. Auffälligkeiten, z.B. dass vor allem alte Menschen oder Kleinkinder, betroffen sind, können wertvolle Hinweise auf die Ausbruchsursache oder das Infektionsvehikel geben. In manchen Ausbruchsuntersuchungen kann es wichtig sein, die Berufsgruppe (z.B. Tierärzte/Tierärztinnen; Waldarbeiter/Waldarbeiterinnen) oder besondere Freizeitaktivitäten (z.B. Jagen) zu erfassen, um Hinweise auf die Ausbruchsursache zu entdecken. Auch die Symptome der Erkrankten, Datum der Erkrankungsbeginne, Erkrankungsbeginn des ersten und des bisher letzten Fall im Ausbruch, Anzahl der Fälle, Anzahl der Hospitalisierungen, Anzahl der Todesfälle und labordiagnostische Ergebnisse gehören zur Beschreibung eines Ausbruchs.
Insbesondere bei Ausbrüchen im Gesundheitswesen und in Gemeinschaftseinrichungen können integrierte Darstellung von Person, Ort und Zeit hilfreich sein. Eine einfache Darstellungsform ist eine Zeitschiene (engl. timeline). Dabei wird jeder Fall in einer Zeile dargestellt. Beispiel für eine Zeitschiene (Haller, 2015):

Tuberkuloseausbrüche erfordern oft viele Kontaktermittlungen. Hier können Netzwerkanalysen hilfreich sein, um Infektionsketten zu visualisieren und nachzuvollziehen. Ein kostenloses Werkzeug zur Netzwerkanalyse und -visualisierung ist NodeXL.
Anhand der Ausbruchsbeschreibung können Hypothesen hinsichtlich der Ausbruchsursache, der Infektionsquelle und des Ausbruchserregers und seinem Übertragungsweg entwickelt werden.
Baustein: Hypothese entwickeln
Um eine Hypothese zum Infektionsvehikel bzw. zur Ausbruchsursache entwickeln zu können, werden alle vorliegenden Informationen herangezogen. Die Entwicklung von Hypothesen in einem Ausbruchsgeschehen ist ein dynamischer Prozess, weil neue Ermittlungserkenntnisse dazu zu neuen Hypothesen oder zur Verwerfung früherer Hypothesen führen. In der frühen Phase einer Ausbruchsuntersuchung werden die Erkrankten ausführlich explorativ befragt. Ziel dieser Befragungen ist es, Gemeinsamkeiten zwischen den Erkrankungsfällen zu entdecken (z.B. gemeinsame Exposition auf einer Familienfeier). Dabei werden Erkrankungsfälle strukturiert, am besten mit einem Fragebogen, befragt. Der Fragebogen kann offene Fragen (Bsp: An welchen Veranstaltungen haben Sie in den 7 Tagen vor Ihrem Erkrankungsbeginn teilgenommen?) und geschlossene Fragen (Bsp: Haben Sie in den 7 Tagen vor Ihrem Erkrankungsbeginn rohes Hackfleisch gegessen?) enthalten. Offene Fragen bieten bei einer explorativen Befragung den Vorteil, dass auch Informationen erfasst werden können, an die die Befragenden vorher nicht gedacht haben und die für die Ausbruchsaufklärung richtungsweisend sein könnten. Sie sind jedoch schwerer zu codieren und auszuwerten als geschlossene Fragen. Befragungen können telefonisch, schriftlich (Fragebogen per Post), online oder face-to-face durchgeführt werden. Bei lebensmittelbedingten Ausbrüchen kommen auch die oben genannten “Shotgun”-Fragebögen (=explorative Fragebögen) zum Einsatz, mit denen der Verzehr einer Vielzahl von Lebensmitteln in den Tagen vor dem Erkrankungsbeginn, aber auch Ernährungsgewohnheiten standardisiert abgefragt werden können.
Aus allen vorliegenden Informationen wird eine Hypothese (oder mehrere) entwickelt, was zu den Erkrankungen geführt haben könnte. Bei einem lebensmittelbedingten Ausbruch wäre die Hypothese, dass der Verzehr eines bestimmten Lebensmittels, z.B. rohes Hackfleisch, in Zusammenhang mit den Erkrankungen im Ausbruchsgeschehen steht (z.B. Salmonellosen). Da bei nosokomialen Ausbrüchen die Personen zu Personen Übertragung im Vordergund steht, ist es Sinnvoll damit als Ausgangshypothese zu starten. Wenn sich trotz implementierter Maßnahmen, oder bei der Ausbruchsuntersuchung Zweifel an diesem Übertragungsweg ergeben, kann die Hypothese entsprechend angepasst werden (Beispiel alle Patienten waren zu Medizinprodukt A exponiert und wurden nicht in räumlicher zeitlicher Nähe behandelt).
Die Hypothesen sollten so früh wie möglich auch in zielgerichtete Präventionsmaßnahmenumgesetzt werden. Dabei kann es sich in Krankenhäusern z.B.um zusätzliche Desinfektionsmaßnahmen, Sperrung von Neuaufnahmen oder das Screening von Patienten handeln. Hierbei ist es unerlässlich, das betroffene Personal mit in die Formulierung der Kontrollmaß-nahmen einzubinden, damit sichergestelltwird, dass diese auch so durchführbar sindund die vorgeschlagenen Änderungenwirklich eine Chance haben, umgesetzt zuwerden. (Zitat Katharina Alpers, Klaus Weist, Tim Eckmanns, Gérard Krause: https://edoc.rki.de/bitstream/handle/176904/948/27SMqNuDowQOs.pdf?sequence=1\&isAllowed=y)
Baustein: Hypothese prüfen
Wenn eine Hypothese entwickelt worden ist, kann diese im nächsten Schritt geprüft werden. Dafür können bei Ausbruchsuntersuchungen analytische epidemiologische Studien durchgeführt werden. Häufig verwendete Studiendesigns sind Kontrollstudien und Fall-Kontroll-Studien. Im Unterschied zu den explorativen Befragungen, die nur bei erkrankten Personen durchgeführt werden, werden bei einer analytischen epidemiologischen Studie sowohl Personen befragt, die erkrankt waren, als auch Personen, die im Ausbruchsgeschehen nicht erkrankt waren. Für analytische Studien werden meist relativ kurze Fragebögen verwendet, die überwiegend geschlossene Fragen (mit den Antwortmöglichkeiten Ja/Nein/ggf. Weiß nicht) enthalten.
Die Durchführung von Kohortenstudien bietet sich bei Ausbrüchen an, die auf einen offensichtlichen gemeinsamen Expositionsort der Erkrankten zurückgeführt werden können (z.B. Ausbrüche nach einer Familienfeier). Unter einer Kohorte versteht man eine definierte, geschlossene Personengruppe, z.B. alle Gäste einer Familienfeier. In einer Kohorte befinden sich Personen, die eine bestimmte Exposition hatte, z.B. auf der Familienfeier Tiramisu gegessen haben, und Personen, die dieser Exposition nicht ausgesetzt waren, also das Tiramisu nicht gegessen haben. Kohortenstudien in Ausbruchsuntersuchungen sind häufig retrospektiv. Zu dem Zeitpunkt, wenn die Studie durchgeführt wird, sind Expositions- und Krankheitsstatus bekannt und können mit Hilfe eines Fragebogens erfasst werden. Die erfassten Daten werden zur Auswertung in sogenannte Vierfeldertafeln eingetragen. Das Erkrankungsrisiko der Exponierten wird dann ins Verhältnis zum Erkrankungsrisiko der Nicht-Exponierten gesetzt, um das Relative Risiko zu berechnen. Das Relative Risiko stellt bei Kohortenstudien das Maß für die Stärke des Zusammenhangs zwischen der Exposition und der Erkrankung dar, d.h. der Zusammenhang ist umso stärker, je höher das Relative Risiko ist. Ein berechnetes Relatives Risiko von 1 bedeutet, dass ein Zusammenhang zwischen der Exposition und den Erkrankungen nicht wahrscheinlich ist, weil das Erkrankungsrisiko der Exponierten in etwa so hoch ist wie das Erkrankungsrisiko der Nicht-Exponierten. Ist das berechnete Relative Risiko größer als 1, weist dies auf einen positiven Zusammenhang zwischen der Exposition und den Erkrankungen hin.
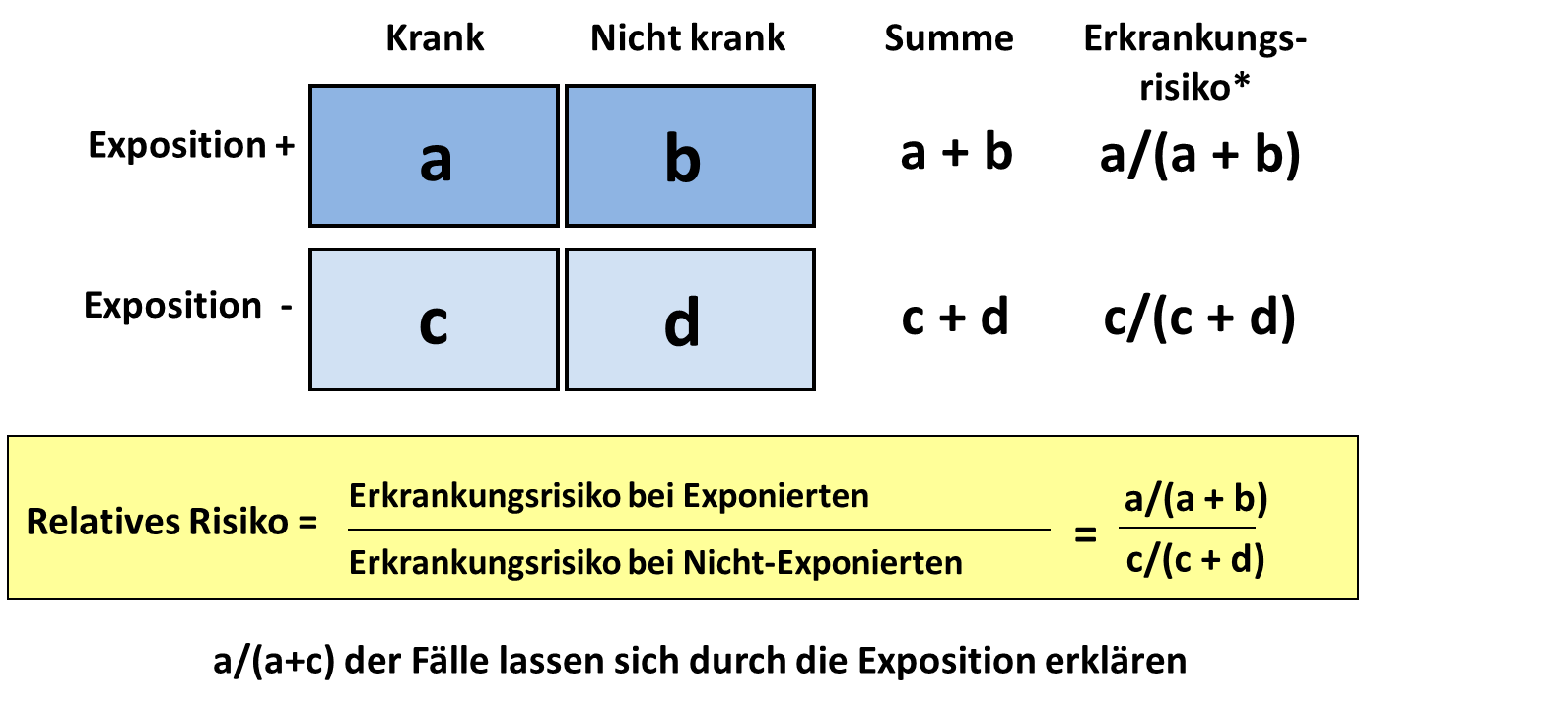
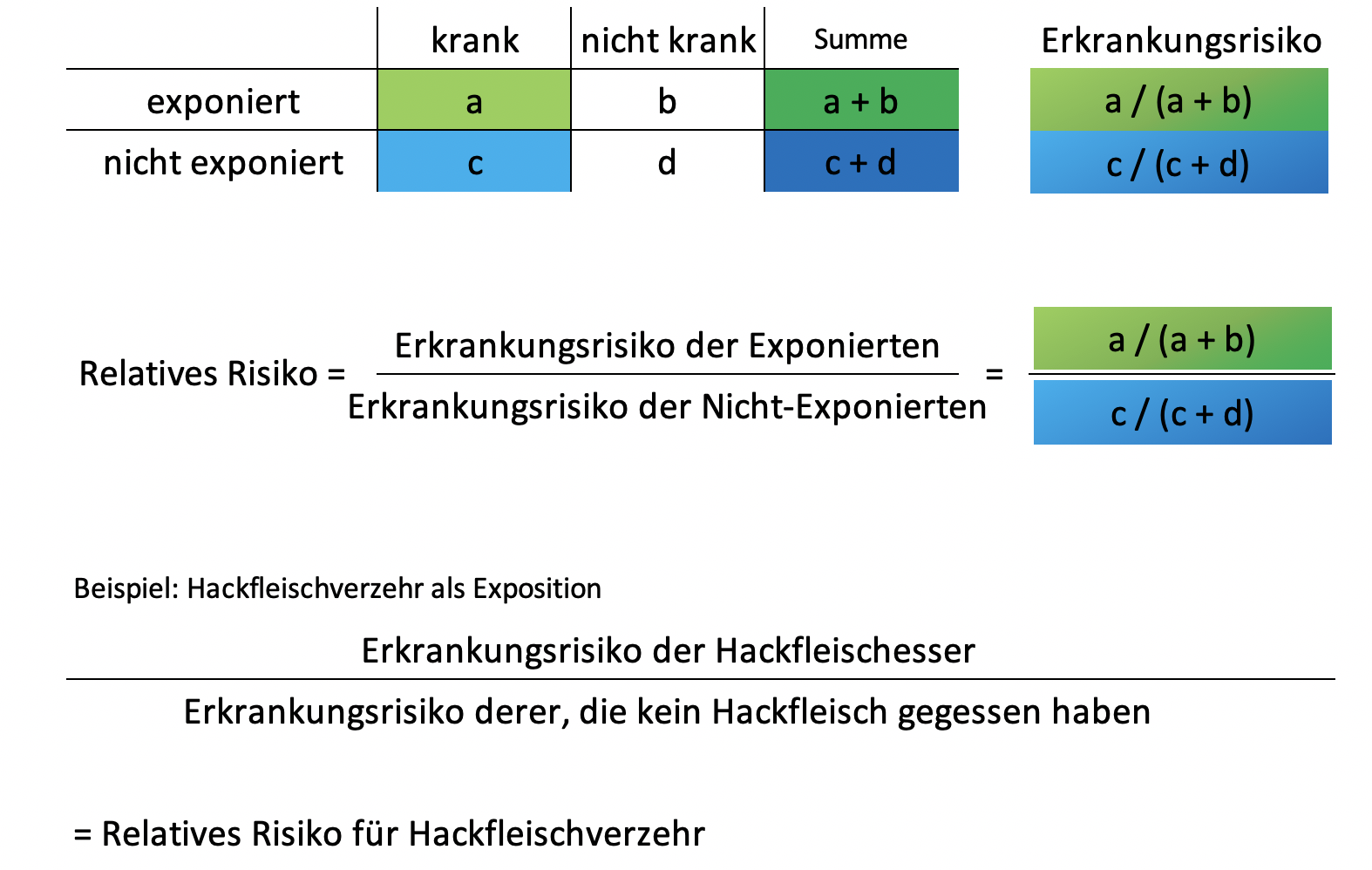
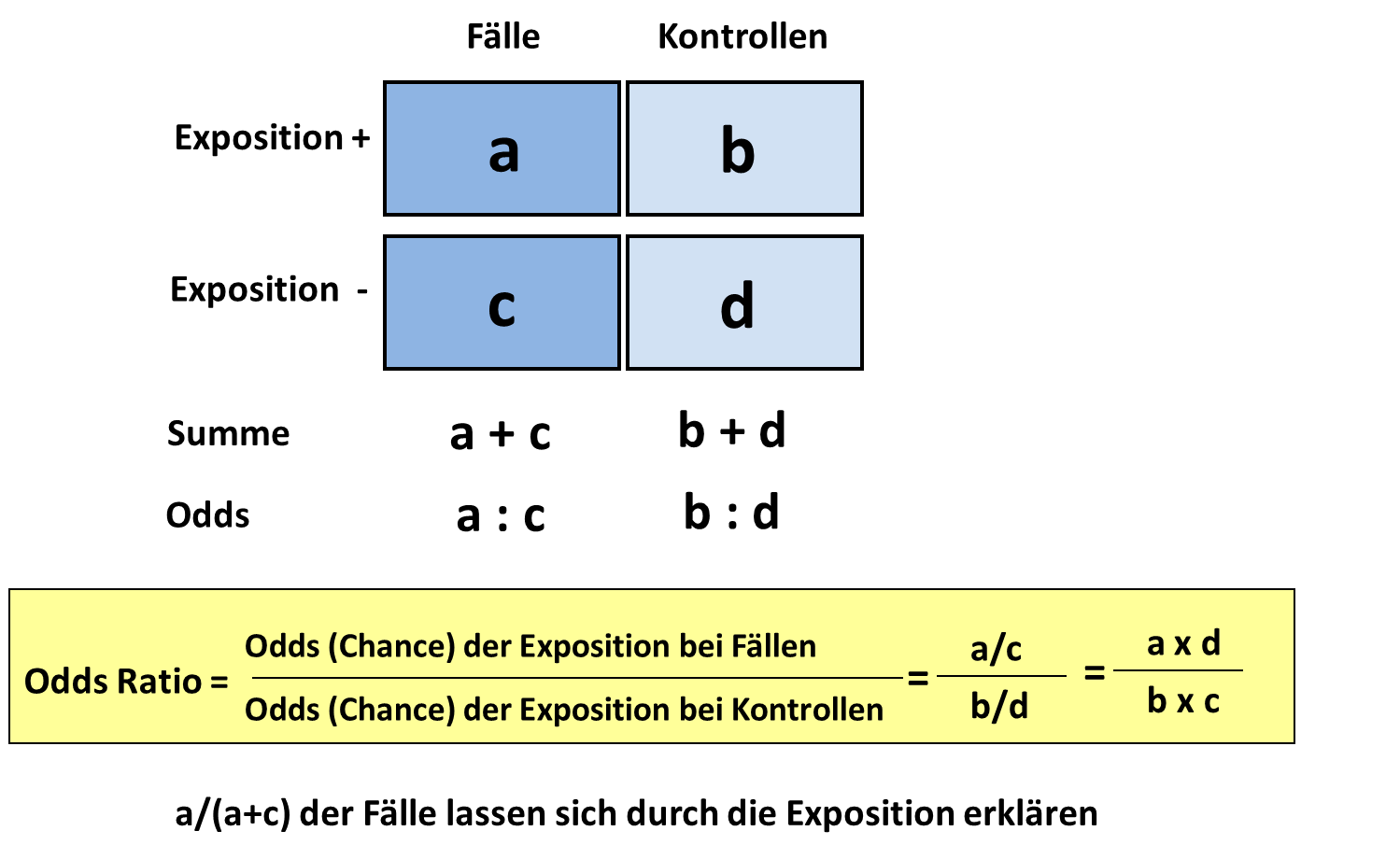
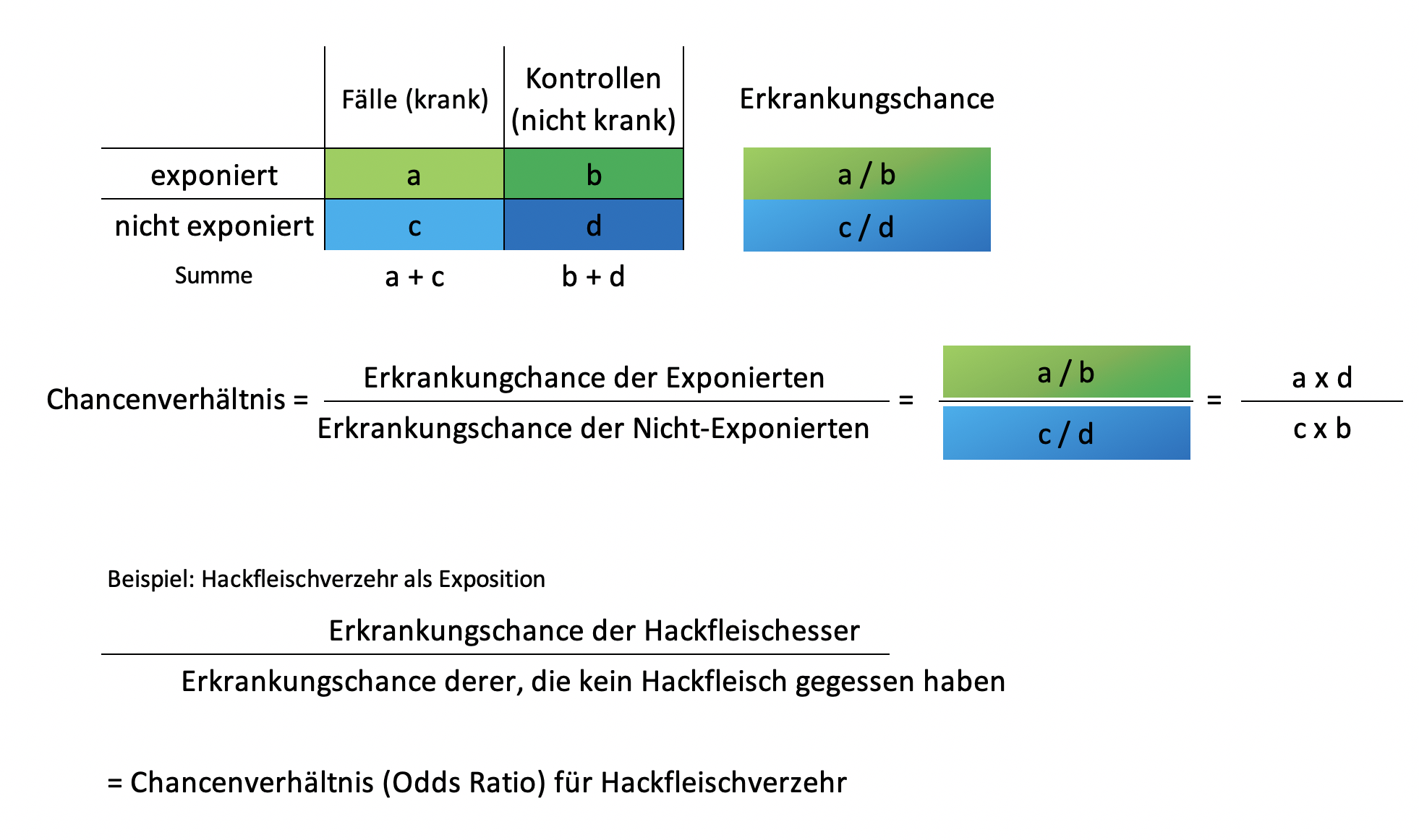
Wenn im Ausbruchsgeschehen die Exposition der Erkrankten nicht auf ein gemeinsames Ereignis oder “Gruppenerlebnis” zurückgeführt werden kann und die Erkrankungsfälle verstreut auftreten, bietet sich die Durchführung einer Fall-Kontroll-Studie an. Im Unterschied zur Kohortenstudie werden die Studienteilnehmenden nach ihrem Erkrankungsstatus ausgewählt. Es wird also nicht mehr die Gruppe, die z.B. auf einer Hochzeitsfeier gemeinsam dem Kuchenbuffet exponiert war, nach Kranken und Gesunden sortiert, sondern man geht von den Erkrankten aus und sucht eine passende Vergleichgruppe. Erkrankte Personen werden als Fälle bezeichnet, nicht-erkrankte Personen als Kontrollen. Nachdem man die Kontrollgruppe beliebig groß wählen kann, würde das Relative Risiko je nach Größe der Kontrollgruppe ein anderes Ergebnis liefern, weil bei dessen Berechnung die Nicht-Kranken jeweils zu den Kranken addiert werden (siehe Abbildung #Relatives Risiko). Als Maß für den Zusammenhang zwischen Exposition und Erkrankungen wird deshalb das Chancenverhältnis (engl. “odds ratio”) berechnet. Eine Verdopplung der Kontrollgruppe kürzt sich beim Chancenverhältnis gegenseitig heraus. Analog zum relativen Risiko wird die Chance (eng. “odds”), bei Exposition zu erkranken durch die Chance geteilt, bei Nichtexposition zu erkranken. Liegt das Chancenverhältnis über Eins (>1) dann erhöht die Exposition (z.B. Verzehr eines Lebensmittels, medizinische Intervention, Anwesenheit auf Station X am Tag Y) die Chance, zu erkranken, verglichen mit Nichtexposition. Eine besondere Herausforderung von Fall-Kontroll-Studien ist es, geeignete Kontrollpersonen zu finden. Kontrollpersonen in einer Fall-Kontroll-Studie müssen dieselbe Gelegenheit gehabt haben, exponiert gewesen zu sein wie die Fälle. Wenn sich beispielsweise bundesweit Infektionen von Kleinkindern mit einem bestimmten Salmonellentyp häufen und man die Hypothese “Ausbruchsvehikel Minisalami” hat, dann könnte man passend zu den Fallpersonen Kleinkinder im gleichen Kreis als Kontrollpopulation wählen (“Salmonella-Panama-Erkrankungen: Zu einem überregionalen Ausbruch bei Kindern durch Minisalami-Sticks,” 2008). Wenn in Gesundheitsämtern die Durchführung einer Fall-Kontroll-Studie geplant ist, wird empfohlen, sich vorher eine statistische Beratung einzuholen oder sich an ihre Landesgesundheitsbehörde oder das RKI zu wenden.
Für lebensmittelbedingte Krankheitsausbrüche bietet das Excel-basierte LINELIST-Werkzeug des RKI die Möglichkeit, Relative Risiken bzw. Odds Ratios zu berechnen (Siehe dazu auch die Veröffentlichung von Werber & Bernard, 2014) (#Verweis auf Grundlagen einfügen, Eintrag Linelist.
Maßzahlen wie Relatives Risiko oder Odds Ratio werden meist mit einem 95%-igen Konfidenzintervall (Vertrauensbereich) angegeben. Wenn die Studie beliebig oft wiederholt werden könnte, würde in 95% der Studien der wahre Wert für die Maßzahl in dem angegebenen Vertraunensbereich liegen. Als Faustregel kann man sich Folgendes merken. Wenn die 1,0 im Konfidenzintervall liegt, dann ist das Ergebnis (Relatives Risiko oder Odds Ratio) wahrscheinlich nicht statistisch signifikant (wenn man einen statistischen Test machen würde).
Nicht in jeder Ausbruchsuntersuchung ist es nötig oder möglich, eine analytische epidemiologische Studie (Kohortenstudie oder Fall-Kontroll-Studie) durchzuführen. Eine analytische Studie sollte dann in Erwägung gezogen werden, wenn die bereits vorliegende Evidenz für den Zusammenhang zwischen einer Exposition (z.B. dem Verzehr eines bestimmten Lebensmittels) und den Erkrankungen nicht ausreichend ist. Bei lebensmittelbedingten Ausbrüchen kann häufig keine labordiagnostische Evidenz mehr erzeugt werden, weil keine Lebensmittel mehr vorhanden sind, die beprobt werden könnten, oder weil ein Erregernachweis im Lebensmittel nicht gelingt. Die ausschließliche Befragung von Erkrankten (ohne Vergleichsgruppe) lässt häufig keine Eingrenzung auf ein einziges Lebensmittel als wahrscheinliches Infektionsvehikel zu, da Lebensmittel, welche von Erkrankten häufig verzehrt werden, auch von Gesunden häufig verzehrt werden, wenn es sich um beliebte Lebensmittel handelt.
Eine analytische Studie ist nur ratsam, wenn eine Hypothese vorliegt, die mit Hilfe der analytischen Studie getestet werden kann. Sie ist jedoch nicht möglich, wenn zu wenige Erkrankte/Fälle (oder Kontrollen) zur Verfügung stehen, so dass das erwartete Ergebnis der Studie nicht aussagekräftig oder belastbar ist. Eine analytische Studie ist hingegen nicht nötig, wenn die vorhandene Evidenz ausreichend ist, um Maßnahmen ergreifen zu können, mit denen der Ausbruch gestoppt und weitere Erkrankungen verhindert werden können.
Bei der Interpretation der Ergebnisse von analytischen Studien sind zufällige Assoziationen, mögliche Verzerrungen (Bias) und Confounding zu berücksichtigen, die in Lehrbüchern der Epidemiologie erklärt sind. Auch ist zu beachten, dass die Interpretation der Odds Ratios in einer Fall-Kontroll-Studie von der Art der Kontrollauswahl abhängt und entweder als relatives Risko, die relative Rate oder der Inzidenz Odds Ratio einer zugrundeliegenden hypothetischen Kohorte interpretiert werden kann (PEARCE, 1993).
Baustein: Maßnahmen ergreifen
Kontrollmaßnahmen müssen im Ausbruchsgeschehen so früh wie möglich ergriffen werden, damit der Ausbruch gestoppt und weitere Erkrankungsfälle verhindert werden können. Kontrollmaßnahmen müssen im Verlauf des Ausbruchsgeschehens ständig evaluiert und gegebenenfalls angepasst werden. Die Kontrollmaßnahmen betreffen eine Fülle von möglichen Aktivitäten, die in den verschiedenen Verordnungen und Gesetzen der Länder und des Bundes aufgeführt sind oder im Ermessen der verantwortlichen Behörden liegen und in anderen Abschnitten genauer dargestellt werden.
Dieser Baustein wird im Rahmen der Ausbruchsuntersuchung explizit erwähnt, da es in der Verantwortung des Ausbruchsteams liegt, alles zu tun, damit nötige Kontrollmaßnahmen eingeleitet werden können. So muss sichergestellt werden, dass Ergebnisse epidemiologischer Untersuchungen zu möglichen Übertragungswegen die dadurch implizierten Kontrollmaßnahmen nach sich ziehen. Häufig liegen die Zuständigkeiten nicht allein im ÖGD, die Umsetzung der implizierten Kontrollmaßnahmen muss aber durch das Ausbruchsteam entsprechend empfohlen und überprüft werden. Ein klassische Beispiel hierführ ist das Abschrauben des Pumpenhebels der “Broad Street Pump” durch John Snow, bei einem Choleraausbruch in London im 19.Jahrhundert. Weitere Kontrollmaßnahmen können z.B. Hygienemaßnahmen, Riegelungsimpfungen, medikamentöse Prophylaxe, Tätigkeitsverbote und bei lebensmittelbedingten Ausbrüchen Lebensmittelrückrufe sein, die von den Lebensmittelüberwachungsbehörden veranlasst werden. Die Implementation von Maßnahmen benötigt stärker als andere Elemente eine solide Rechtfertigungsbasis im Sinne einer konsequenten Beweisführung der Ausbruchsursache um auch spätere juristische Konsequenzen zu minimieren.
Baustein: Kommunizieren
Allgemein
Zur effektiven Kommunikation im Rahmen eines Ausbruchsmanagements gehören sowohl die Information aller Akteure untereinander, als auch die Information der Fachöffentlichkeit und der Öffentlichkeit sowie die Informationsweitergabe an und durch die Medien. Die Weltgesundheitsorganisation schreibt: “Effektive Risikokommunikation ist ein wesentliches Element des Ausbruchsmanagements. Wenn die Öffentlichkeit von einer tatsächlichen oder potentiellen Gesundheitsbedrohung bedroht ist, sind die Behandlungsmöglichkeiten möglicherweise begrenzt, direkte Interventionen können Zeit in Anspruch nehmen und es stehen nur wenige Ressourcen zur Verfügung. Eine proaktive Kommunikation ermutigt die Öffentlichkeit, sich schützendes Verhalten anzueignen, erleichtert die Überwachung der Krankheit, verringert die Verwirrung und ermöglicht eine bessere Nutzung der Ressourcen - alles notwendige Voraussetzungen für eine wirksame Reaktion. […] Indem eine Bevölkerung und Partner auf ein Infektionskrankheitsrisiko aufmerksam gemacht werden, nimmt die Erfassung potenzieller Fälle zu, werden schützende Verhaltensweisen angenommen, ist die Verwirrung begrenzt und werden die Kommunikationsressourcen eher konzentriert. Eine wirksame Kommunikation kann dazu beitragen, die Ausbreitung einer Krankheit zu begrenzen und letztlich Leben zu retten.” (World Health OrganizationOutbreak CommunicationPlanning Guide, 2008).
Kommunikation muss dabei situations- und lagebedingt sein. Bei einem kleinen Ausbruch kann es beispielsweise sein, dass gar keine Pressemitteilung verfasst, oder erst nach Presseanfrage eine Mitteilung herausgegeben wird. Während eines großen Ausbruchsgeschehen ist jedoch die Verunsicherung der Bevölkerung groß. Hier ist von Anfang an “mit einem massiven Bedarf an Informationen und Kommunikation zu rechnen” (“Epidemisch bedeutsame Lagen erkennen, bewerten und erfolgreich bewältigen,” 2019) diesem sollte man frühzeitig mit adäquaten Methoden der Krisenkommunikation und unter Nutzung aller Medien erfolgen. Hierbei kann es hilfreich sein die zuständige Presseabteilung bereits vorab mit Informationen zu versorgen, sodass im Bedarfsfall schnell auf Anfragen reagiert werden kann.
Wichtig ist zudem die zeitnahe Information anderer beteiligter Behörden sowie die Weitergabe von für die Bearbeitung des Ausbruchsgeschehens wichtiger neuer Informationen. Hinweise zu involvierten Akteuren gibt beispielsweise das Dokument “National Pandemiplan Teil I” des RKI oder der Leitfaden Management lebensmittelassoziierter Infektionen das Landes Baden-Würrtemberg.
Gesetzlich vorgeschriebene Meldewege (§§ 6 und 7 Infektionsschutzgesetz) müssen, wie bereits im Kapitel Vorbereitung (Dokumente @Editor: Bitte internen Link einfügen) beschrieben, eingehalten werden (IfSG). In der Regel werden die benötigten Meldebögen durch die Länder bereitgestellt. Meldebögen, die nach den Internationalen Gesundheitsvorschriften (IGV) eine mögliche gsundheitliche Notlage von internationaler Tragweite beinhalten (IfSG §12) können auf der Internetseite des RKI heruntergeladen werden [Meldebogen nach IGV].
Das RKI stellt bei Bedarf Meldungen in das Europäische Frühwarnsystem “Early Warning and Response System (EWRS)” ein und leitet die dort eingstellten Informationen an die zuständigen Landesbehörden weiter.
Wesentliche Prinzipien einer effektiven Kommunikation
Die WHO hat informative Dokumente zur Kommunikation in Ausbrüchen veröffentlicht (2013, 2018a, 2018b; World Health OrganizationOutbreak CommunicationPlanning Guide, 2008). Dabei sind die unten ausgeführten fünf Punkte wesentliche Eckpunkte, die insbesondere bei schwerwiegenden Ausbrüchen berücksichtigt werden sollten.
1. Vertrauen aufbauen
”Als Grundlage für eine wirksame Kommunikation ist es das wichtigste Ziel, das Vertrauen der Öffentlichkeit in die für die Bekämpfung des Ausbruchs und die Herausgabe von Informationen über den Ausbruch Verantwortlichen aufzubauen, zu erhalten oder wiederherzustellen. Diese besondere Bedeutung des Vertrauens hat sich in allen Kulturen, politischen Systemen und auf allen Ebenen der wirtschaftlichen Entwicklung herausgestellt, denn Vertrauen entsteht aus der öffentlichen Wahrnehmung der Motive, der Ehrlichkeit und der Kompetenz von Behörden. Das Vertrauen der Öffentlichkeit, dass eine Regierung oder Behörde in erster Linie zum Schutz der Gesundheit handelt, beeinflusst die Einhaltung der empfohlenen Kontrollmaßnahmen und beschleunigt somit die Eindämmung des Ausbruchs. Das Vertrauen in die Ehrlichkeit der Behörden und das Vertrauen darauf, dass beunruhigende Tatsachen nicht heruntergespielt oder verschwiegen werden, verringert die Angst der Öffentlichkeit während der unvermeidlichen Ungewissheit eines Ausbruchs. Das Vertrauen darauf, dass die Behörden kompetent sind und die Kontrolle haben, hilft weiter, Reaktionen zu verhindern, die die sozialen und wirtschaftlichen Auswirkungen eines Ausbruchs verschlimmern.
2. Frühzeitig informieren
Die frühzeitige Information über einen Ausbruch stellt die beste Strategie dar. Da menschliches Verhalten fast immer eine Rolle bei der Ausbreitung eines Ausbruchs spielt, trägt eine frühzeitige Kommunikation zur frühzeitigen Eindämmung in einer Situation bei, in der jeder Tag zählt. Ebenso wichtig ist, dass eine frühzeitige Bekanntgabe das Vertrauen der Öffentlichkeit gewinnt, dass die Behörden offen melden, was sie wissen, wenn sie es wissen, und damit die Erwartung wecken, dass Informationen nicht verschwiegen werden. Die erste Mitteilung über einen Ausbruch ist oft die wichtigste. Naturgemäß ist die Bekanntmachung eines Ausbruchs ein aktuelles Thema, welches die Aufmerksamkeit der Medien und der Öffentlichkeit auf sich zieht und ein großes Alarmpotential beinhaltet. Die Art und Weise, wie diese erste Ankündigung gehandhabt wird - wenn das Rampenlicht am intensivsten ist - kann den Empfang aller nachfolgenden Nachrichten beeinflussen. Eine verspätete Bekanntgabe eines Ausreißers erweckt den Eindruck, dass die Verantwortlichen Informationen verheimlichen und vielleicht mehr darum bemüht sind, die Angst der Öffentlichkeit und den Verlust von Einkünften aus Handel und Tourismus zu verhindern, als die öffentliche Gesundheit zu schützen. Der daraus resultierende Vertrauensverlust kann sich gleich zu Beginn als nicht wiedergewinnbar erweisen.
3. Transparent sein
Transparenz kennzeichnet die Beziehung zwischen den Ausbruchsverantwortlichen und der Öffentlichkeit. Transparenz kann definiert werden als Kommunikation, die offen, leicht verständlich, vollständig und genau ist. Im Allgemeinen führt größere Transparenz zu mehr Vertrauen. Transparenz bietet viele Vorteile, u.a. zeigt sie, wie die Verantwortlichen für Krankheitsausbrüche selbst in einer Zeit der Unsicherheit und vieler Unbekannter systematisch nach Antworten suchen. Transparenz kann auch Managementmängel aufdecken, sie bietet einen starken Anreiz für abwägende und rechenschaftspflichtige Entscheidungen. Transparenz hat auch Grenzen, da einige Informationen, wie z.B. vertrauliche Patientendaten, aus ethischen Gründen nicht veröffentlicht werden sollten. Der Schlüssel ist die Abwägung solcher Bedenken gegen das Recht, den Bedarf und den Wunsch der Öffentlichkeit nach verlässlichen Informationen. Die Festlegung der Grenzen der Transparenz kann von Ausbruch zu Ausbruch variieren, aber wenn diese zu einer Entschuldigung für die Geheimhaltung werden, wird das wahrscheinlich zu einem Vertrauensverlust der Öffentlichkeit führen.
4. Die Bedenken der Öffentlichkeit respektieren
Die Öffentlichkeit hat Anspruch auf Informationen, die ihre Gesundheit und die ihrer Angehörigen betreffen. Öffentliche Bedenken sollten als legitim behandelt, untersucht und als eine Kraft respektiert werden, die die Auswirkungen eines Ausbruchs beeinflusst. Frühe Risikokommunikation war didaktisch, indem sie die Fakten darlegte, der Öffentlichkeit sagte, wie sie reagieren sollte, und dann alle anderen Reaktionen als “irrational” bezeichnete. Heute wird eine effektive Risikokommunikation als Dialog zwischen Fachexperten und der Öffentlichkeit angesehen.
Ein Ausbruch erregt die Aufmerksamkeit vieler verschiedener Öffentlichkeiten - Risikogruppen, Patienten und ihre Familien und Nachbarn, Medien, Forscher, Gemeindeleiter, Handelspartner und Touristen - und betrifft sie auf sehr unterschiedliche Weise. Die Kommunikation über einen Ausbruch funktioniert am besten, wenn die Sichtweise all dieser Öffentlichkeiten bei der Entscheidung darüber, was und wie man es sagt, berücksichtigt wird. Sobald Entscheidungen getroffen sind, sollten die Partner sich um aktuelle Informationen in koordinierter und konsistenter Weise bemühen. Bei der Ankündigung von Entscheidungen zu Beginn eines Ausbruchs wird die Presse hilfreich sein, insbesondere wenn das Management des Ausbruchs transparent ist. Aber Journalisten können sich schnell gegen die eigene Institution wenden, wenn sie das Gefühl haben, getäuscht worden zu sein.
5. Im Voraus planen
Die Planung ist für eine effektive Kommunikation über einen Ausbruch unerlässlich, und dennoch wird sie selten durchgeführt. Die Kommunikationsplanung bei Ausbrüchen muss von Anfang an Teil der Planung des Ausbruchsmanagements sein. Unter den Notfallbedingungen eines Ausbruchs kann die Kommunikation nicht ideal sein, wenn ihre Prinzipien erst in letzter Minute in der Eile der Informationsveröffentlichung berücksichtigt werden. Gleichzeitig ist eine nicht im Voraus geplante Kommunikation über einen Ausbruch nicht unbedingt zum Scheitern verurteilt. Viele der von SARS betroffenen Länder hatten keine Kommunikationspläne, kommunizierten aber sehr effektiv mit der Öffentlichkeit. Andere haben große Fehler gemacht - und teuer bezahlt; diese hätten vermieden werden können, wenn die Kommunikationsfragen im Voraus berücksichtigt worden wären.” (Outbreak Communication, 2004) [Kommunikation im National Pandemieplan Teil I].
Kommunikationsplan/-strategie
Wie beschrieben sollte die Krisenkommunikationsstrategie im Zeitraum zwischen großen Ausbrüchen etabliert und geprüft werden: Behörden und andere Akteure “müssen ihre Kommunikationsmittel-, -inhalte und -strategien miteinander abstimmen. (…) Damit diese Abstimmungen im Krisenfall auch komplikationslos funktionieren können, wird ein regelmäßiges Training empfohlen.”
Das Centre of Disease Control (Bensyl et al., n.d.) hat hierzu hilfreiche Hinweise veröffentlicht:
-
”Ermittlung und Benennung eines Sprechers oder einer dauerhaft erreichbaren Kontaktstelle, die als primärer Anprechpartner für das Untersuchungsteam fungiert. Indem die Kommunikationsrolle auf eine oder wenige Personen konzentriert wird, wird die Effizienz des Teams optimiert. Dies minimiert auch das Potenzial für Verwirrung oder Missverständnisse, indem es die Konsistenz der Nachrichtenübermittlung während der gesamten Untersuchung gewährleistet.
- Geben Sie mündliche Briefings und schriftliche Mitteilungen ab, wie dies angezeigt sein könnte.
- Schriftliche Berichte können für verschiedene Zwecke angepasst werden, z.B. für die formelle Übermittlung von Empfehlungen, die Erfüllung institutioneller Anforderungen an die Dokumentation, die Bereitstellung von Unterlagen für künftige Referenzen und die Erleichterung der raschen Verbreitung von Untersuchungsergebnissen an die ersuchende Behörde, Interessenvertreter, wissenschaftliche Kollegen und andere.
- Vor der Abreise sollte das Untersuchungsteam der ersuchenden Behörde und den lokalen Interessenvertretern einen vorläufigen schriftlichen Bericht und eine mündliche Einweisung geben, in dem alle Aktivitäten dokumentiert, die Ergebnisse mitgeteilt und Empfehlungen vermittelt werden. Ein abschließender, detaillierterer Bericht könnte zu einem späteren Zeitpunkt vorgelegt werden, insbesondere wenn zusätzliche Analysen und Studien geplant sind.
- Kurzberichte, die rasch in Bulletins zum öffentlichen Gesundheitswesen veröffentlicht werden (z.B. Wochenbericht zur Morbidität und Mortalität), können dazu beitragen, die Kollegen auf das Problem aufmerksam zu machen.”
Trainingsmaterial
Grundlagen und Trainings zu Risiko- und Krisenkommunikation im Gesundheitsbereich werden u. a. von der WHO (Risikokommunikations-Guideline) und dem ECDC angeboten (A literature review on effective risk communication for the prevention and control of communicable diseases in Europe. (2013). ; [
- WHO. Communicating Risk in Public Health Emergencies. A WHO Guideline for Emergency Risk Communication (ERC) policy and practice. (2018).</span>](http://www.who.int/risk-communication/guidance/download/en/ “ 61. WHO. Communicating Risk in Public Health Emergencies. A WHO Guideline for Emergency Risk Communication (ERC) policy and practice. (2018).”)). Deutschsprachige Materialien bietet der Leitfaden Krisenkommunikation des BMI oder das von der EU finanzierte HealthC-Projekt. (62 .The Health C project. Improving crisis communication skills in health emergency management.; 63. Bundesministerium-des-Inneren. Leitfaden Krisenkommunikation. (2014).)
#